Hôm nay 9-12, Hội đồng đạo đức y sinh thuộc Bộ Y tế sẽ họp trước khi vắc xin Nanocovax được đưa ra thử nghiệm trên người.
- Nhiều người dân tình nguyện thử vắc xin COVID-19 của Việt Nam
- Ai được tiêm vắcxin COVID-19 trước tiên?
- Vaccine Covid-19 Việt Nam ở giai đoạn nào?
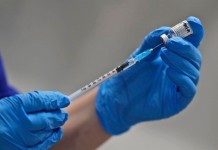
 Nghiên cứu sản xuất vắc xin chống COVID-19 tại Công ty cổ phần công nghệ sinh học dược Nanogen – Ảnh: DUYÊN PHAN
Nghiên cứu sản xuất vắc xin chống COVID-19 tại Công ty cổ phần công nghệ sinh học dược Nanogen – Ảnh: DUYÊN PHAN
Từ ngày 10-12, Công ty cổ phần công nghệ sinh học dược Nanogen phối hợp với Học viện Quân y (Bộ Quốc phòng), bắt đầu quá trình thử nghiệm vắc xin (vaccine) trên người. Đây là một bước tiến đáng ghi nhận, mở ra kỳ vọng về một loại vắc xin mang thương hiệu “made in Việt Nam”.
Bác sĩ NGUYỄN PHƯƠNG THỦY – trưởng phòng y khoa (Công ty cổ phần công nghệ sinh học dược Nanogen, gọi tắt Nanogen), một trong số các thành viên tham gia quá trình sản xuất vắc xin từ ngày đầu – nói: “Từ khi virus corona ở Vũ Hán (Trung Quốc) có chiều hướng bùng phát mạnh trên phạm vi toàn cầu, nhiều nơi vào cuộc sản xuất vắc xin, đó cũng là lúc ý tưởng sản xuất vắc xin của chúng tôi được manh nha.
Nhưng phải đến đầu tháng 5-2020, bằng việc đầu tư nguồn lực con người; nâng cấp trang thiết bị vật tư, cơ sở hạ tầng để nghiên cứu, bào chế vắc xin… Nanogen cùng với ba đơn vị khác ở Việt Nam mới được Bộ KH-CN phê duyệt ‘danh mục nhiệm vụ khoa học công nghệ cấp quốc gia đột xuất phòng, chống dịch COVID-19′”.
Công nghệ tái tổ hợp
* Nanogen sản xuất vắc xin dựa trên công nghệ protein tái tổ hợp. Yếu tố nào làm nên sự khác biệt của công nghệ này?
– Hiện nay trên thế giới có ba hướng phát triển vắc xin chính gồm vắc xin mRNA (vắc xin RNA truyền tin, Mỹ), vắc xin tiểu đơn vị protein và vắc xin véctơ. Trong khi phần lớn các vắc xin của các hãng dược phẩm trên thế giới đều theo hướng RNA và vắc xin véctơ thì vắc xin của Nanogen là protein tái tổ hợp.
Nhược điểm lớn nhất của loại vắc xin protein tái tổ hợp này là vấn đề thời gian, bởi phải tạo dòng và chọn lọc trên tế bào. Tuy vậy nó lại mang ưu điểm là tạo được đáp ứng miễn dịch tốt, độ an toàn cao, ít tác dụng phụ, điều kiện bảo quản thuận lợi hơn nhiều loại vắc xin khác.
* Kết quả thử nghiệm lâm sàng trên động vật trước đó đạt kết quả như thế nào, thưa bác sĩ?
– Chúng tôi đã thực hiện thử nghiệm tiền lâm sàng về đáp ứng miễn dịch trên chuột Balb/c (chủng chuột bạch tạng nuôi cấy trong phòng thí nghiệm); chuột Hamster (chuột đuôi cụt, còn gọi là chuột đất vàng) và khỉ. Các thử nghiệm này cho thấy vắc xin có khả năng sinh miễn dịch tốt; thử nghiệm về độc tính trên chuột nhắt, chuột lang, thỏ và khỉ đều cho thấy vắc xin đảm bảo tính an toàn.
Cụ thể, trên chuột và khỉ vắc xin chỉ gây ngứa nhẹ ở vị trí tiêm (bắp) và hết sau 30 phút. Đặc biệt, giải phẫu chuột tiêm vắc xin không thấy cơ quan nội tạng nào bị tổn thương.
Tình nguyện viên từ 12-75 tuổi
* Nhiều người dân mong muốn được đăng ký làm tình nguyện viên thử nghiệm vắc xin. Các điều kiện cần thiết và đăng ký ra sao?
– Tất cả các thông tin này sẽ được công bố đầy đủ sau cuộc họp của Hội đồng đạo đức (Bộ Y tế) vào ngày 9-12 tới. Tuy nhiên trước mắt người dân có thể hiểu giai đoạn đầu tiên (giai đoạn 1) sẽ thử nghiệm trên 40 tình nguyện viên, đều do Học viện Quân y (Bộ Quốc phòng) phụ trách tuyển chọn.
Về tuổi từ 18-50 tuổi, đảm bảo khỏe mạnh (không mắc các bệnh truyền nhiễm, mãn tính…), phải được sàng lọc qua một số cận lâm sàng cơ bản và đặc biệt không phải người có nguy cơ cao nhiễm COVID-19.
Ở giai đoạn 2 và giai đoạn 3 chỉ có thay đổi về độ tuổi tình nguyện viên từ 12-75 tuổi (tuổi sức đề kháng yếu hơn). Trong đó, giai đoạn 2 dự kiến thực hiện vào giữa tháng 1-2021 ở TP.HCM (có thể tại Viện Pasteur), với quy mô thử nghiệm trên 400-600 tình nguyện viên.
Quá trình thử nghiệm lâm sàng có thể kéo dài sáu tháng, có thể nhanh hơn nếu các kết quả thử nghiệm thuận lợi. Và làm sao để vào khoảng tháng 5-2021 vắc xin có thể được tiêm chủng đại trà.
* Nếu việc thử nghiệm vắc xin này thành công, đơn vị có ước tính là sẽ sản xuất được bao nhiêu vắc xin?
– Với quy mô hiện tại chúng tôi có thể sản xuất 2 triệu liều vắc xin/năm. Và chúng tôi đang tính toán đầu tư nâng cấp công suất sản xuất lên 30 triệu liều/năm, trong tương lai có thể đạt con số 50 triệu liều/năm.
* Về giá sản phẩm khi đưa ra thị trường, có thông tin đơn vị dự kiến áp dụng mức giá 5 USD/mũi tiêm, mỗi người tiêm 2 mũi sẽ chi phí 10 USD (hơn 200.000 đồng). Đây có phải là mức giá cuối cùng?
– Đến nay mức giá cuối cùng của vắc xin chưa được chốt, nhưng chắc chắn không quá 500.000 đồng/liều (đang dự tính từ 200.000 – 300.000 đồng/liều). Theo liệu trình, mỗi người cần tiêm hai liều, cách nhau 28 ngày và phải tiêm nhắc lại sau một năm.
Chúng tôi sẽ cố gắng cân đối làm sao vừa không bị lỗ, vừa đảm bảo túi tiền để mọi người dân Việt Nam có thể tiếp cận được. Đồng thời, cố gắng để Nanocovax (tên gọi của vắc xin) được đưa vào danh mục thuốc được BHYT chi trả nhằm giảm bớt gánh nặng chi phí cho người dân.
* Tính khả thi cũng như kỳ vọng về loại vắc xin này ra sao?
– Tất nhiên cũng như người dân, chúng tôi rất kỳ vọng đây là vắc xin COVID-19 đầu tiên mang thương hiệu “made in Việt Nam” được đưa ra thị trường, với mục tiêu cung cấp đủ vắc xin phục vụ người Việt, chung tay cùng Chính phủ đẩy lùi dịch bệnh COVID-19. Và chúng tôi đang nỗ lực hết sức nhằm đáp ứng sớm nhất có thể nhu cầu của người dân, xã hội…
| Những người đầu tiên tiêm vắc xin ngừa COVID-19 của Việt Nam
Hôm nay 9-12, Hội đồng đạo đức y sinh thuộc Bộ Y tế sẽ họp trước khi vắc xin Nanocovax được đưa ra thử nghiệm trên người. Đây sẽ là những người đầu tiên được tiêm vắc xin ngừa COVID-19 (thử nghiệm) tại Việt Nam. Theo ông Nguyễn Ngô Quang – phó cục trưởng Cục Khoa học công nghệ và đào tạo, Bộ Y tế, những người như sau có thể đăng ký tham gia thử nghiệm vắc xin: 1. Là người tình nguyện, tham gia nghiên cứu theo nguyện vọng cá nhân, không chịu áp lực nào về sức khỏe, tài chính, hành chính… 2. Đã đọc và hiểu kỹ bảng thông tin nghiên cứu, nguyên tắc của cuộc thử nghiệm. 3. Có đủ năng lực hành vi, trên 18 tuổi. 4. Khỏe mạnh, không mắc bất kỳ bệnh cấp/mãn tính nào. 5. Các chỉ số huyết học, sinh hóa bình thường. Ngoài ra, còn một số tiêu chí đặc thù, sẽ được thông qua tại cuộc họp ngày 9-12. Người tham gia nghiên cứu sẽ được mua bảo hiểm sức khỏe theo quy định hiện hành ở Việt Nam cũng như trên thế giới. Ở giai đoạn 1 của thử nghiệm lâm sàng trên người, tiêu chí theo dõi quan trọng nhất là chỉ số an toàn của vắc xin. Dự kiến sẽ có từ 40-60 người tham gia thử nghiệm đợt này, tiêm 2 loại liều dự kiến là 50 và 75mg. Ở giai đoạn 2 của cuộc thử nghiệm, dự kiến sẽ bắt đầu vào tháng 4-2021, khi đã có từ 50% kết quả của thử nghiệm giai đoạn 1, nhóm nghiên cứu sẽ theo dõi tính sinh miễn dịch của vắc xin. Thử nghiệm giai đoạn 2 sẽ tiêm ít nhất trên 400 người tình nguyện. Tại Học viện Quân y, đã có một khu vực được thiết lập để theo dõi người tiêm thử nghiệm Nanocovax sau tiêm 72 giờ, nhằm đảm bảo các chỉ số theo dõi là đồng nhất. Ngày 10-12, Học viện Quân y sẽ thông báo chính thức việc tuyển tình nguyện viên tham gia cuộc thử nghiệm và chuẩn bị trong vòng một tuần để có thể tiêm mũi Nanocovax đầu tiên vào ngày 17-12. L.ANH |
| Tiếp tục nghiên cứu hiệu lực bảo vệ
Ông Nguyễn Ngô Quang – phó cục trưởng Cục Khoa học công nghệ và đào tạo (Bộ Y tế): Có ba chỉ tiêu khi đánh giá một vắc xin, đó là tính an toàn, tính sinh miễn dịch và hiệu lực bảo vệ. Vắc xin của Nanogen đang làm dựa trên protein tái tổ hợp, sau đó can thiệp vào bộ gen để sản sinh ra kháng thể. Điều này khác hoàn toàn với việc dùng kháng thể (tức dùng virus bất hoạt hoặc virus sống). Bước đầu ở góc độ cơ quan quản lý nhà nước và các nhà khoa học đánh giá là an toàn, có tính sinh miễn dịch sau sản sinh kháng thể. Tuy nhiên về hiệu lực bảo vệ kéo dài bao lâu cần phải có thời gian nghiên cứu. |
| 4 nguyên nhân sản xuất vắc xin ở Việt Nam về đích muộn
Theo Nanogen, thời điểm mà Việt Nam bắt tay nghiên cứu vắc xin ngừa COVID-19 không muộn hơn so với nhiều nước, nhưng lại “về đích” muộn hơn bởi nhiều nguyên nhân khách quan. Cụ thể, Việt Nam không có nhiều ca nhiễm COVID-19 để lấy mẫu làm ảnh hưởng đến quá trình thử nghiệm, không có phòng thí nghiệm đủ lớn với các công nghệ hiện đại để thử nghiệm vắc xin trên động vật, chưa có nhiều nghiên cứu lâm sàng pha 1 để tham khảo và cuối cùng là chưa có các quy định cụ thể về quy trình thủ tục hướng dẫn sản xuất, đăng ký sử dụng vắc xin COVID-19. Với mục tiêu “gối đầu” thử nghiệm giai đoạn 2 trong thời gian sớm nhất, Nanogen cho biết đang xây dựng nhiều phương án cho thử nghiệm lâm sàng giai đoạn 2 dựa trên kết quả dự kiến của giai đoạn 1 theo chỉ đạo của Bộ Y tế. |
Theo HOÀNG LỘC – THÙY DƯƠNG – tuoitre.vn